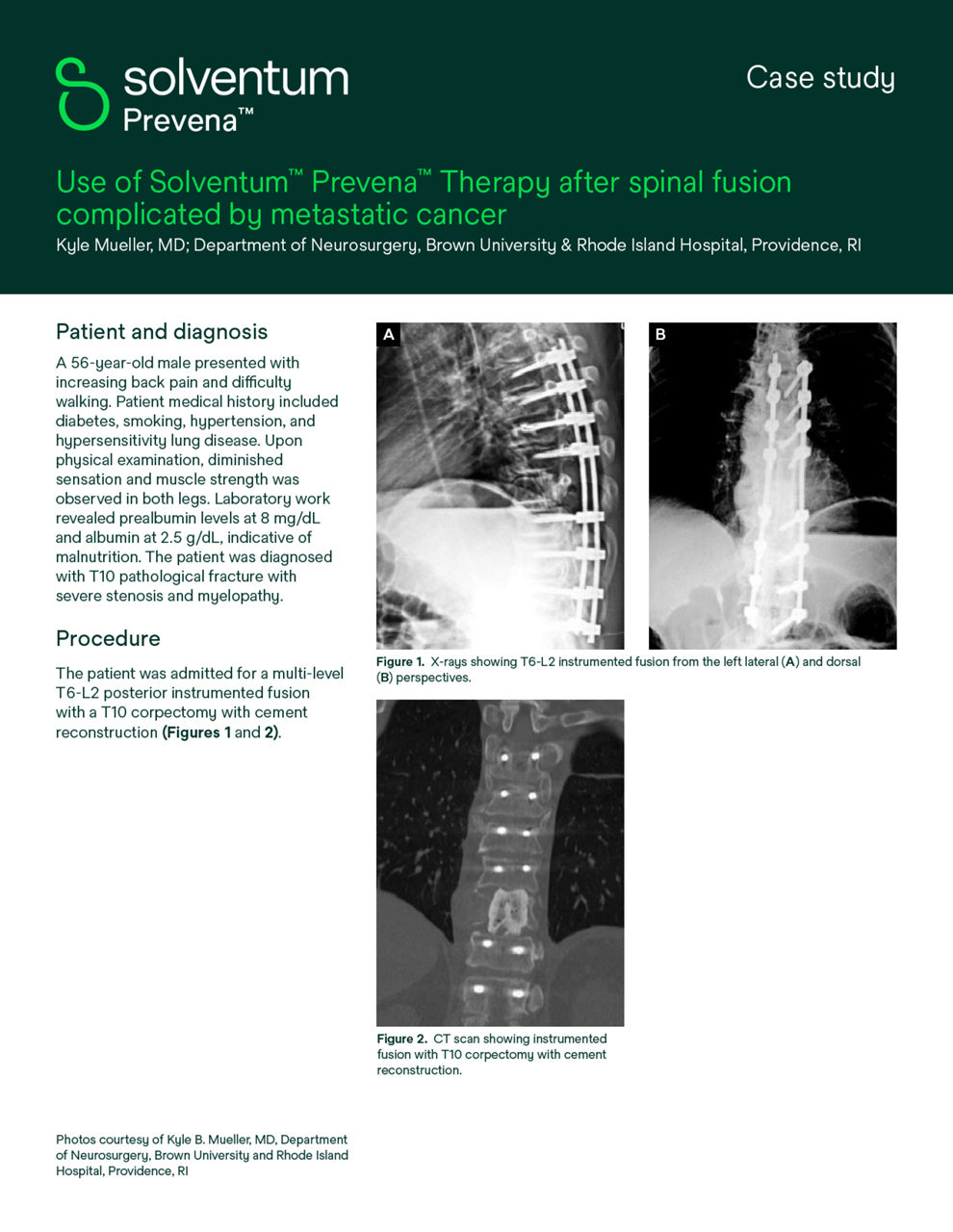
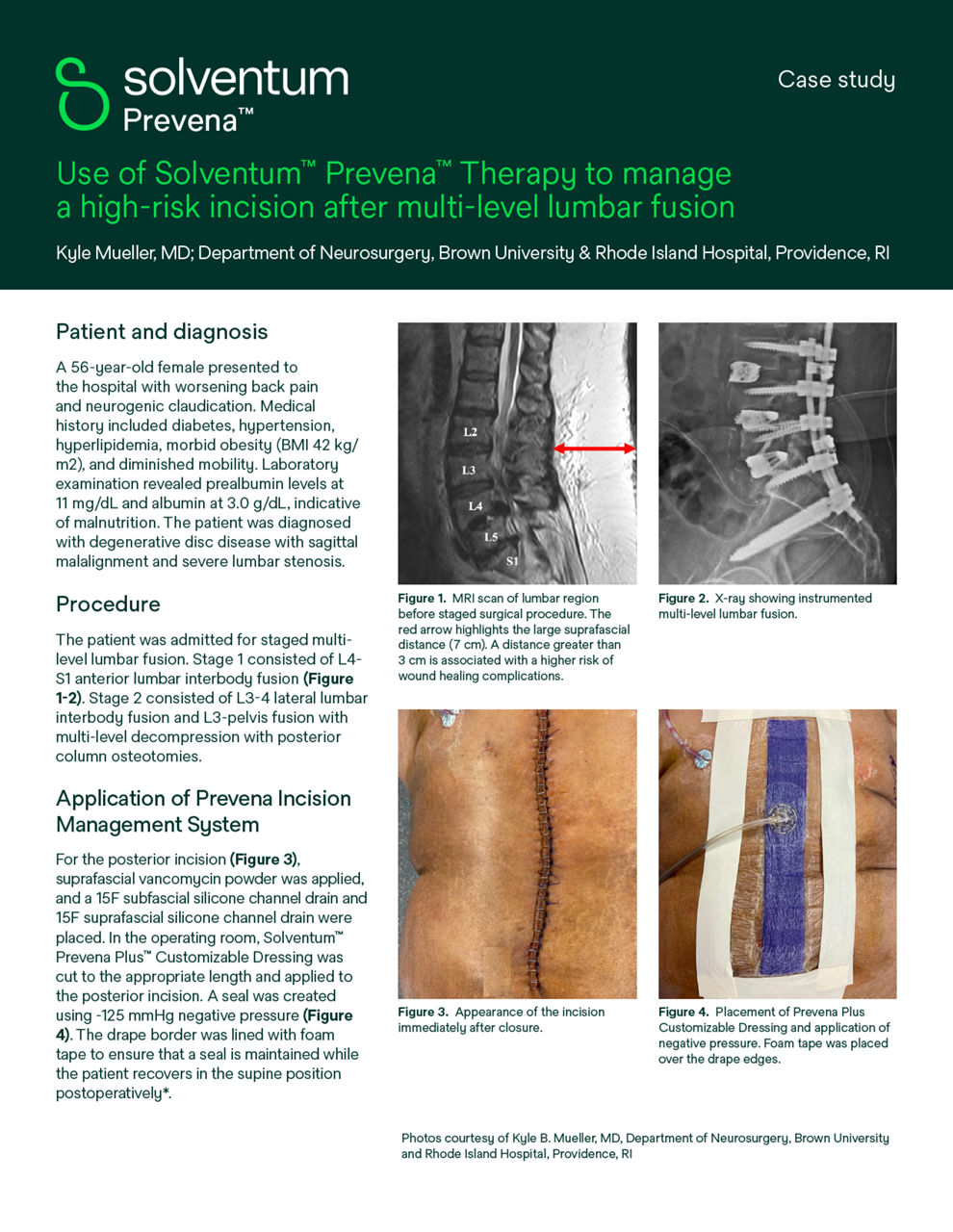
Thérapie 3M Prevena pour la chirurgie vertébrale
Gestion proactive des risques (GPR)
Accédez à des ressources complètes pour intégrer la GPR dans votre pratique avec la thérapie 3M Prevena, aidant à élever votre niveau de soins aux patients avec des avantages postopératoires prouvés.
Ressources vidéo pour la thérapie Prevena
Études de cas
Découvrez notre sélection de cas d'études soigneusement choisis, mettant en avant des chirurgiens et des experts renommés qui démontrent l'efficacité de la thérapie Prevena dans divers contextes chirurgicaux.
Pour aller plus loin
REMARQUE:
Des indications spécifiques, des contre-indications, des avertissements, des précautions et des informations de sécurité existent pour ces produits et ces thérapies. Veuillez consulter un clinicien et lire les instructions d'utilisation du produit avant toute utilisation. Ce document est destiné aux professionnels de santé. Med-Surg-300 - Janvier 2025 - Prevena sont des marques déposées de la Société Solventum. Tous droits réservés. Photos non contractuelles. Le Système PREVENA™ est un DM de Classe IIa. Marquage CE2797. Fabriqué par KCI USA. Distribué par Solventum France, 1 Parvis de l’Innovation,95006 Cergy-Pontoise cedex.
Indication(s) d'utilisation / Utilisation prévue : Approuvé par la FDA américaine : seulement pour une utilisation aux États-Unis :
Pansement Prevena utilisé avec les unités de thérapie Prevena : Les unités de thérapie PREVENA™ 125 et PREVENA PLUS™ 125 gèrent l'environnement des incisions chirurgicales fermées et éliminent les fluides de l'incision chirurgicale par l'application d'une pression négative continue de -125mmHg. Lorsqu'elles sont utilisées avec des pansements PREVENA™ compatibles commercialisés légalement pendant jusqu'à sept jours, les unités de thérapie PREVENA™ 125 et PREVENA PLUS™ 125 sont destinées à aider à réduire l'incidence des séromes et, chez les patients présentant un risque élevé d'infections postopératoires, à aider à réduire l'incidence des infections superficielles du site chirurgical dans les plaies de classe I et de classe II.
Limitations :
- L'appareil n'est pas destiné à traiter les infections du site chirurgical ou les séromes.
- La sécurité et l'efficacité chez la population pédiatrique (<22 mois) n'ont pas été évaluées.
- La sécurité et l'efficacité dans les plaies de classe III (contaminées) et de classe IV (sales/infectées) n'ont pas été démontrées. De plus, les plaies chirurgicales de classe IV ne sont pas censées être fermées principalement, et le dispositif en question ne doit être utilisé que sur des incisions chirurgicales fermées.
- Il n'a pas été démontré que l'appareil réduit les infections profondes de l'incision et de l'espace organique du site chirurgical.
- Il n'a pas été démontré que l'appareil est efficace pour réduire l'incidence des infections du site chirurgical et des séromes dans toutes les procédures chirurgicales et toutes les populations de patients; par conséquent, l'appareil ne peut pas être recommandé pour une utilisation systématique afin de réduire l'incidence des infections du site chirurgical et des séromes.
- Veuillez vous référer à la section "Résumé des informations cliniques" pour les procédures chirurgicales spécifiques et les populations de patients incluses dans les études cliniques. Les chirurgiens doivent continuer à suivre les "Directives du Centre pour le contrôle et la prévention des maladies pour la prévention des infections du site chirurgical" et les "Directives de l'American College of Surgeons et de la Surgical Infection Society: Surgical Site Infection Guidelines" pour les meilleures pratiques en matière de prévention des infections du site chirurgical. Approuvé par la FDA américaine : Pansements/Systèmes (Pansements Prevena utilisés avec les unités NPWT compatibles Solventum - ActiVAC, Ulta, et RX4) et pays applicables hors États-Unis qui utilisent les indications américaines : Les systèmes de gestion des incisions PREVENA™, PREVENA PLUS™, PREVENA DUO™ et PREVENA RESTOR™ sont destinés à gérer l'environnement des incisions chirurgicales qui continuent de drainer après une fermeture par suture ou agrafage en maintenant un environnement fermé et en éliminant les exsudats par l'application d'une thérapie par pression négative.
Références :
- Akhter, AS, et al. Negative pressure wound therapy in spinal fusion patients. Int Wound J. 2020; 1-6. https://doi.org/10.1111/iwj.13507
- Berríos-Torres, S. I., Umscheid, C. A., Bratzler, D. W., Leas, B., Stone, E. C., Kelz, R. R., Reinke, C. E., Morgan, S., Solomkin, J. S., Mazuski, J. E., Dellinger, E. P., Itani, K. M., Berbari, E. F., Segreti, J., Parvizi, J., Blanchard, J., Allen, G., Kluytmans, J. A., Donlan, R., & Schecter, W. P. (2017). Centers for Disease Control and Prevention guideline for the prevention of surgical site infection, 2017. JAMA Surgery, 152(8), 784. https://doi.org/10.1001/jamasurg.2017.0904
- Ban, K. A., Minei, J. P., Laronga, C., Harbrecht, B. G., Jensen, E. H., Fry, D. E., Itani, K. M. F., Dellinger, P. E., Ko, C. Y., & Duane, T. M. (2017). American College of Surgeons and Surgical Infection Society: Surgical Site Infection Guidelines, 2016 update. Journal of the American College of Surgeons, 224(1), 59–74. https://doi.org/10.1016/j.jamcollsurg.2016.10.029