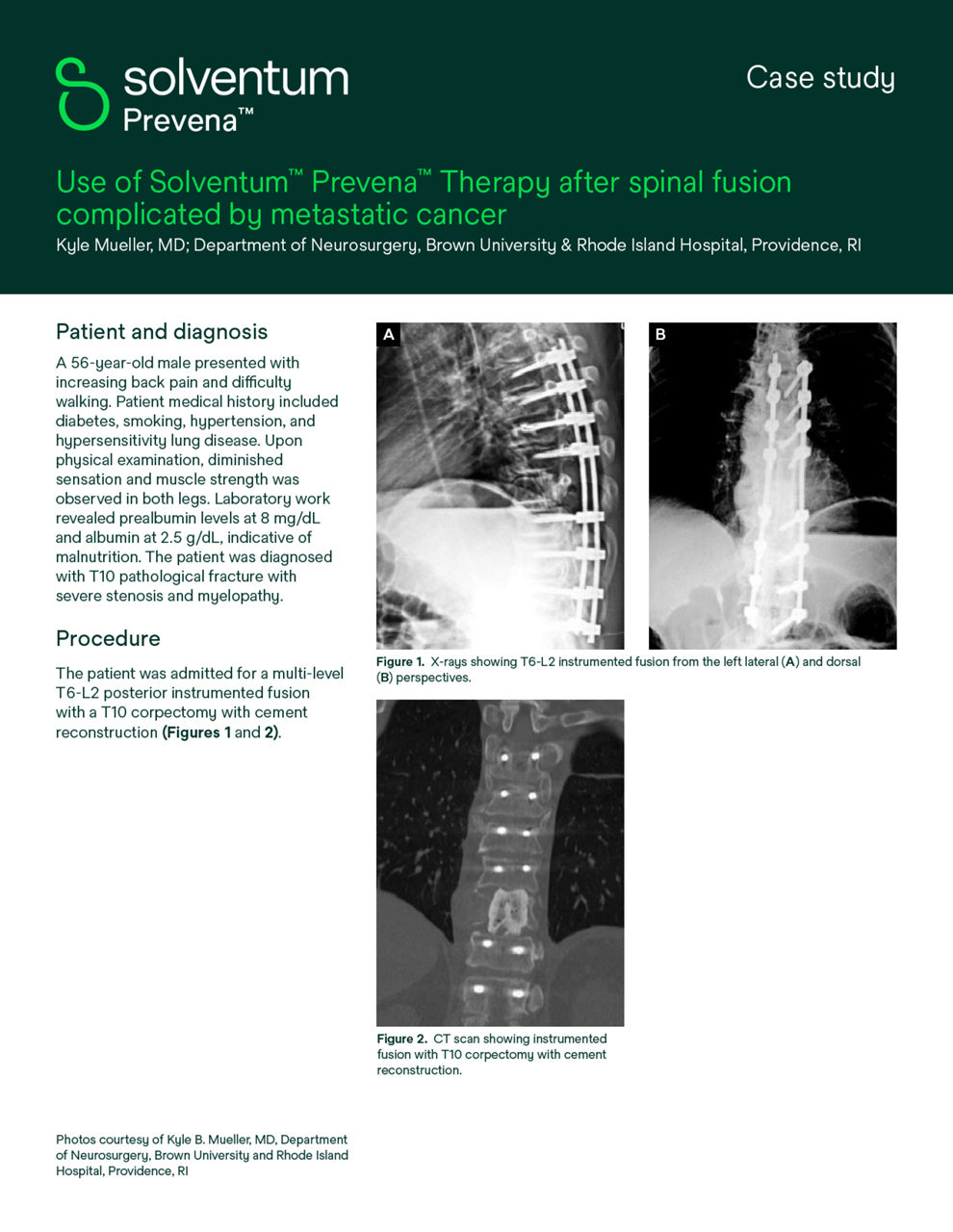
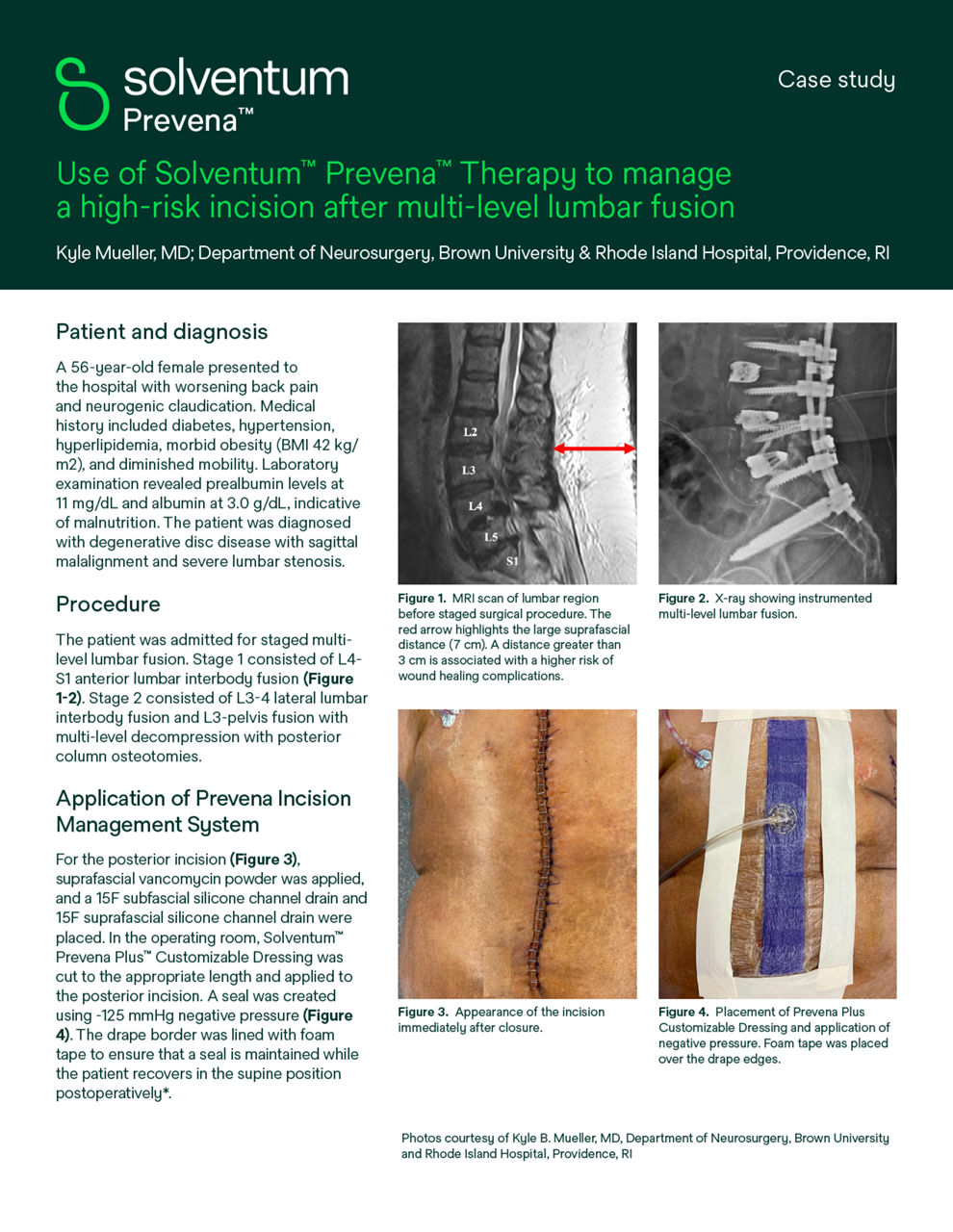
3M Prevena 治療用於脊椎手術
積極風險管理(PRM)
利用 Prevena 治療,獲得全面資源以將 PRM 實施到您的實踐中,透過已證實的術後效益提升您的病人護理標準。
Prevena 治療視頻資源
案例研究
探索我們精選的案例研究集合,其中包括了受尊敬的外科醫生和專家們,展示了Prevena治療在各種手術情境中的效果。
探索更多
注意:
這些產品和治療存在特定的適應症、限制、禁忌、警告、注意事項和安全信息。使用前請諮詢臨床醫師並查閱產品使用說明書。僅限醫生使用。
使用指示 / 預期用途:美國 FDA 批准:僅限在美國使用:
Prevena 裹料配合 Prevena 治療裝置使用: PREVENA™ 125 與 PREVENA PLUS™ 125 治療裝置通過應用 -125mmHg 持續負壓,管理閉合手術切口的環境並將液體從手術切口中抽出。當與合法上市的兼容 PREVENA™ 裹料一起使用最多七天時,PREVENA™ 125 與 PREVENA PLUS™ 125 治療裝置旨在幫助減少血清腫的發生;並且在高風險術後感染的患者中,幫助減少 I 級和 II 級傷口表淺手術部位感染的發生。
限制:
- 該裝置不旨在治療手術部位感染或血清腫。
- 在兒科人群中(<22 歲)的安全性和有效性尚未評估。
- 在 III 級(污染)和 IV 級(骯髒/感染)傷口中的安全性和有效性尚未證明。此外,IV 級手術傷口預計不會首先閉合,且該裝置應僅用於閉合的手術切口上。
- 尚未證明該裝置可以減少深層切口和器官空間手術部位感染。
- 尚未證明該裝置在所有手術程序和患者人群中有效降低手術部位感染和血清腫的發生率;因此,不建議常規使用該裝置以減少手術部位感染和血清腫的發生。
- 有關具體手術程序和患者人群的臨床研究信息,請參閱「臨床信息摘要」部分。外科醫生應繼續遵循「疾病控制和預防中心手術部位感染預防指南」2 和「美國外科學院和外科感染學會:手術部位感染指南」3 中的最佳實踐。美國 FDA 批准的裹料/系統(Prevena 裹料配合兼容的 Solventum NPWT 單元 - ActiVAC, Ulta, 和 RX4)和適用於依賴美國指示的 OUS 國家:PREVENA™, PREVENA PLUS™, PREVENA DUO™, 和 PREVENA RESTOR™ 切口管理系統旨在管理縫合或用訂書釘閉合後仍持續排液的手術切口的環境,通過應用負壓傷口治療來保持閉合環境並移除滲出液。
參考文獻:
- Akhter, AS, et al. 脊柱融合患者的負壓傷口治療。國際傷口期刊。2020; 1-6. https://doi.org/10.1111/iwj.13507
- Berríos-Torres, S. I., Umscheid, C. A., Bratzler, D. W., Leas, B., Stone, E. C., Kelz, R. R., Reinke, C. E., Morgan, S., Solomkin, J. S., Mazuski, J. E., Dellinger, E. P., Itani, K. M., Berbari, E. F., Segreti, J., Parvizi, J., Blanchard, J., Allen, G., Kluytmans, J. A., Donlan, R., & Schecter, W. P. (2017). 疾病控制和預防中心2017年手術部位感染預防指南。JAMA 外科,152(8), 784. https://doi.org/10.1001/jamasurg.2017.0904
- Ban, K. A., Minei, J. P., Laronga, C., Harbrecht, B. G., Jensen, E. H., Fry, D. E., Itani, K. M. F., Dellinger, P. E., Ko, C. Y., & Duane, T. M. (2017). 美國外科學院和外科感染學會:2016年更新的手術部位感染指南。美國外科學院雜誌,224(1), 59–74. https://doi.org/10.1016/j.jamcollsurg.2016.10.029