3M Prevena 治療病人資訊
什麼是Prevena治療?
您的醫療服務提供者已為您提供了3M™ Prevena™ 治療系統 - 一個便攜式的單次使用裝置 - 以支持您的康復之旅。這項先進技術包括一種醫療設備,使用真空輔助閉合(V.A.C.®)治療,對您的傷口或切口施加控制的負壓。
開始您的Prevena治療之旅
病人影片
了解更多有關您的Prevena治療裝置 - 它的工作原理,日常佩戴和照顧您的系統的小貼士,以及如何閱讀和排除您裝置上的警報。
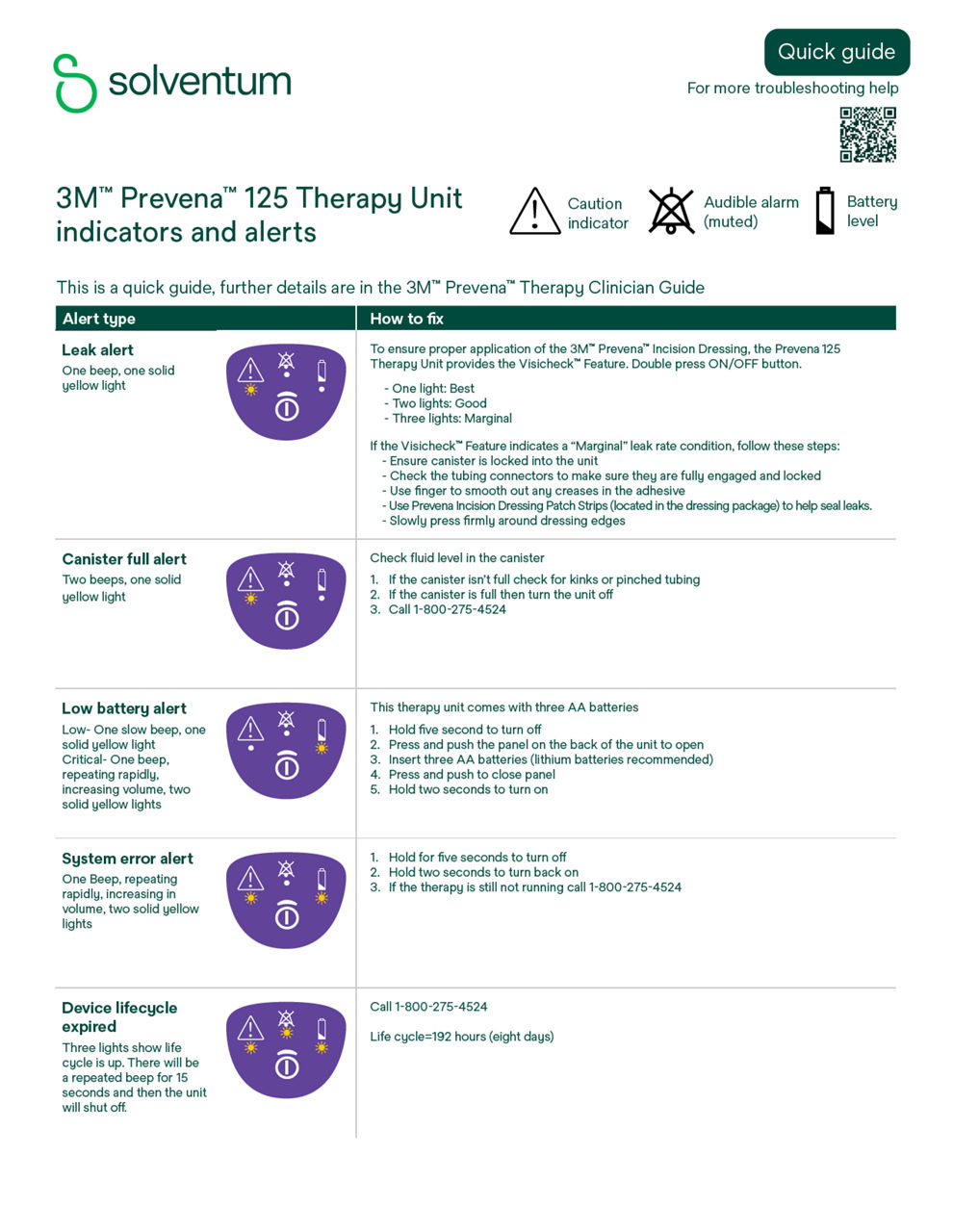
3M Prevena 125 治療裝置
常見問題
如有疑問,請參考Prevena治療病人指南 (PDF, 770.19 KB)或警示指南 (PDF, 1.50 MB),或聯繫您的醫療服務提供者。
請按照您的醫療提供者的指示,佩戴系統至指定時間,屆時您的醫生將會移除敷料。治療單元將在7天後自動關機。
通常不更換敷料。請遵循您的健康護理提供者的指示。
這個便攜式裝置應該依照您的健康照護提供者的指示,持續保持開啟。該單元可以穿在衣服內或外,並包括一個帶有可調節帶子的攜帶箱,因此您可以多種方式使用。
請將您的治療裝置放置在安全的地方,避免軟管扭結或被夾住,並確保裝置不會被拉離桌面或掉落到地板上。
此治療單元附帶三節AA尺寸電池,並且不能充電。建議您準備額外的電池。如果電池用完,請參閱Prevena治療病人指南了解如何更換電池。
若經您的醫療服務提供者清楚說明同意後,可以快速地淋浴,但要淺淺的。保持治療裝置遠離直接水花。不要將敷料浸泡在水中。使用毛巾擦乾時,小心不要弄亂敷料。
病人影片
進一步了解您的Prevena治療裝置 - 它的工作原理、日常佩戴和照顧系統的提示,以及如何讀取和排除您裝置上的警報。
3M Prevena Plus 125 治療裝置
常見問題
每位病患都是獨一無二的,您的醫療保健提供者應為您提供明確的治療期限資訊。您應按照醫療保健提供者的指示佩戴該系統。作為指南,用於封閉手術切口的Prevena 125 治療裝置最長可持續7天。可用於封閉切口和開放性傷口的Prevena Plus 125 治療裝置最長可持續14天。
更換敷料的頻率將取決於您的治療。您的健康照護提供者應該向您提供有關您的敷料是否需要更換,以及如何更換的信息。請確保您遵循健康照護提供者的指示。如果您正在使用Prevena Plus和V.A.C.敷料治療開放性傷口,敷料更換應每48-72小時進行一次。如果您使用Prevena敷料治療閉合的手術切口,則通常不需要更換敷料,敷料可持續使用長達7天。如果您使用Prevena Restor敷料治療閉合的手術切口,則通常不需要更換敷料,敷料可持續使用長達14天。
請參閱 Prevena 治療病人指南 (PDF, 770.19 KB) 或 警示指南 (PDF, 1.50 MB) 如果您有任何問題,請撥打我們的免費客服電話 0800 980 8880,或如果在愛爾蘭,撥打免費電話 1800 33 33 77。
此便攜式裝置應按照醫生的指示保持開啟狀態。該裝置可以穿在衣服內外,並附有可調節帶子的攜帶包,因此您可以多種方式使用。
請將您的治療裝置放置在安全的地方,確保軟管不會被扭結或壓扁,並且避免裝置從桌子上掉落或跌落到地板上。
Prevena Plus 125 治療裝置具有可充電電池並附有充電器。如果您將外出較長時間,請攜帶您的充電器。為了方便起見,建議您在睡覺時充電您的治療裝置電池。
如果您的醫療服務提供者同意,可以快速輕柔地沖個淋浴。請避免治療單元直接接觸水流。不要將敷料浸入水中。使用毛巾擦乾時,要小心不要弄亂敷料。
Prevena治療支持手術康復
如果您正在为手术做准备,思考如何保护术后切口以帮助您的恢复至关重要。您的切口将通过缝合或使用钉书针等方式关闭,但手术切口带来的风险可能会影响您的愈合:
正確的切口護理對於及時康復和維持您的生活品質至關重要。Prevena 治療系統可以成為您護理計劃的一部分。這個易於使用的一次性系統應用溫和的負壓來保護和管理您的切口,以幫助減少手術部位併發症的風險,例如感染。Prevena 治療的工作原理包括:
- 切口管理:創建一個隔離外部污染物的屏障並保護切口部位
- 液體管理:移除液體和感染物質
- 切口支持:有助於保持切口邊緣緊密結合
對於皮膚脆弱、對壓克力和/或羥膠黏合劑或銀過敏的患者,或那些出血風險增加的患者,應謹慎使用Prevena治療。有關詳細信息,請參閱患者指南,並諮詢您的醫生。
NOTE:
Specific indications, limitations, contraindications, warnings, precautions and safety information exist for these products and therapies. Please consult a clinician and product instructions for use prior to application. Rx only.
Indication(s) For Use / Intended Use: US FDA Cleared: Only for Use in the United States:
Prevena Dressing used with Prevena Therapy Units: PREVENA™ 125 and PREVENA PLUS™ 125 Therapy Units manage the environment of closed surgical incisions and remove fluid away from the surgical incision via the application of -125mmHg continuous negative pressure. When used with legally marketed compatible PREVENA™ dressings for up to seven days, PREVENA™ 125 and PREVENA PLUS™ 125 Therapy Units are intended to aid in reducing the incidence of seroma; and in patients at high risk for post-operative infections, aid in reducing the incidence of superficial surgical site infection in Class I and Class II wounds.
Limitations:
- The device is not intended to treat surgical site infection or seroma.
- Safety and effectiveness in pediatric population (<22 years old) have not been evaluated.
- Safety and effectiveness in Class III (Contaminated) and Class IV (Dirty/Infected) wounds have not been demonstrated. Furthermore, Class IV surgical wounds are not expected to be closed primarily, and the subject device should only be used on closed surgical incisions.
- The device has not been demonstrated to reduce deep incisional and organ space surgical site infections.
- The device has not been demonstrated to be effective in reducing the incidence of surgical site infection and seroma in all surgical procedures and patient populations; therefore, the device may not be recommended for routine use to reduce the incidence of surgical site infection and seroma.
- Please refer to the ‘Summary of Clinical Information’ section for the specific surgical procedures and patient populations included in the clinical studies. Surgeons should continue to follow the ‘Centers for Disease Control and Prevention Guideline for the Prevention of Surgical Site Infection’4 and the ‘American College of Surgeons and Surgical Infection Society: Surgical Site Infection Guidelines’5 for best practices in preventing surgical site infection. US FDA Cleared: Dressings/ Systems (Prevena Dressings used with compatible Solventum NPWT units - ActiVAC, Ulta, and RX4) and applicable OUS countries that leverage US Indication: The PREVENA™, PREVENA PLUS™, PREVENA DUO™, and PREVENA RESTOR™ Incision Management Systems are intended to manage the environment of surgical incisions that continue to drain following sutured or stapled closure by maintaining a closed environment and removing exudates via the application of negative pressure wound therapy.
參考文獻:
- Zimlichman E, Henderson D, Tamir, et al. Health care-associated Infections a meta-analysis of costs and financial impact on the U.S. health care system. JAMA Intern ed.2013;173(22):20-46.
- Magill SS, Edwards JR, Bamberg W, et al. Multistate point-prevalence survey of health care-associated Infections. N Engl JMed. 2014;370:1198-208.
- Shepard J, Ward W, Milstone A, et al. Financial impact of surgical site infections on hospitals. The hospital management perspective. JAMA Surg. 2013;148(10):907-914. doi:10.1001/jamasurg.2013.2246
- Berríos-Torres, S. I., Umscheid, C. A., Bratzler, D. W., Leas, B., Stone, E. C., Kelz, R. R., Reinke, C. E., Morgan, S., Solomkin, J. S., Mazuski, J. E., Dellinger, E. P., Itani, K. M., Berbari, E. F., Segreti, J., Parvizi, J., Blanchard, J., Allen, G., Kluytmans, J. A., Donlan, R., & Schecter, W. P. (2017). Centers for Disease Control and Prevention guideline for the prevention of surgical site infection, 2017. JAMA Surgery, 152(8), 784. https://doi.org/10.1001/jamasurg.2017.0904 opens in a new tab
- Ban, K. A., Minei, J. P., Laronga, C., Harbrecht, B. G., Jensen, E. H., Fry, D. E., Itani, K. M. F., Dellinger, P. E., Ko, C. Y., & Duane, T. M. (2017). American College of Surgeons and Surgical Infection Society: Surgical Site Infection Guidelines, 2016 update. Journal of the American College of Surgeons, 224(1), 59–74. https://doi.org/10.1016/j.jamcollsurg.2016.10.029opens in a new tab